Nitơ là một chất đã được sử dụng rất nhiều trong công nghiệp, và nó đóng vai trò quan trọng trong nhiều ngành công nghiệp hiện nay. Vậy Nitơ là gì? Những đặc điểm và tác dụng của khí Nitơ như thế nào. Hãy cùng hoccungthukhoa.vn tìm hiểu Nitơ là gì và những điều đặc biệt xoay quanh Nitơ nhé!
1. Tìm hiểu Nitơ là gì?
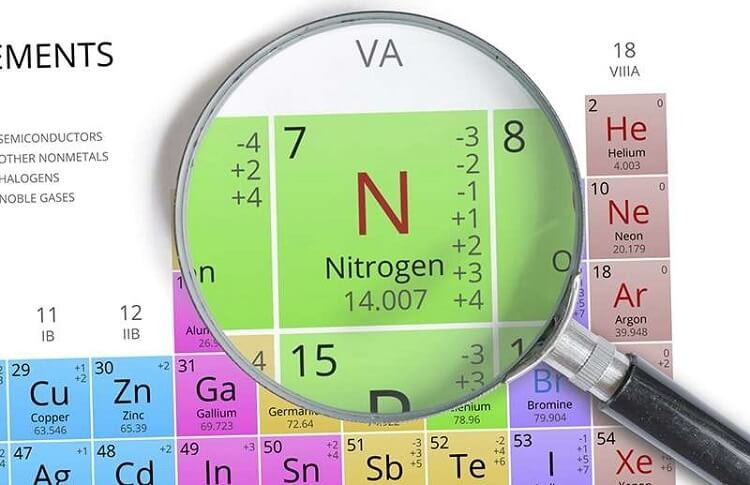
Nitơ là thành phần chính của khí quyển, đóng góp vào việc bảo vệ Trái Đất khỏi tác động và hủy hoại của bức xạ mặt trời. Nitơ có công thức hóa học là N2.
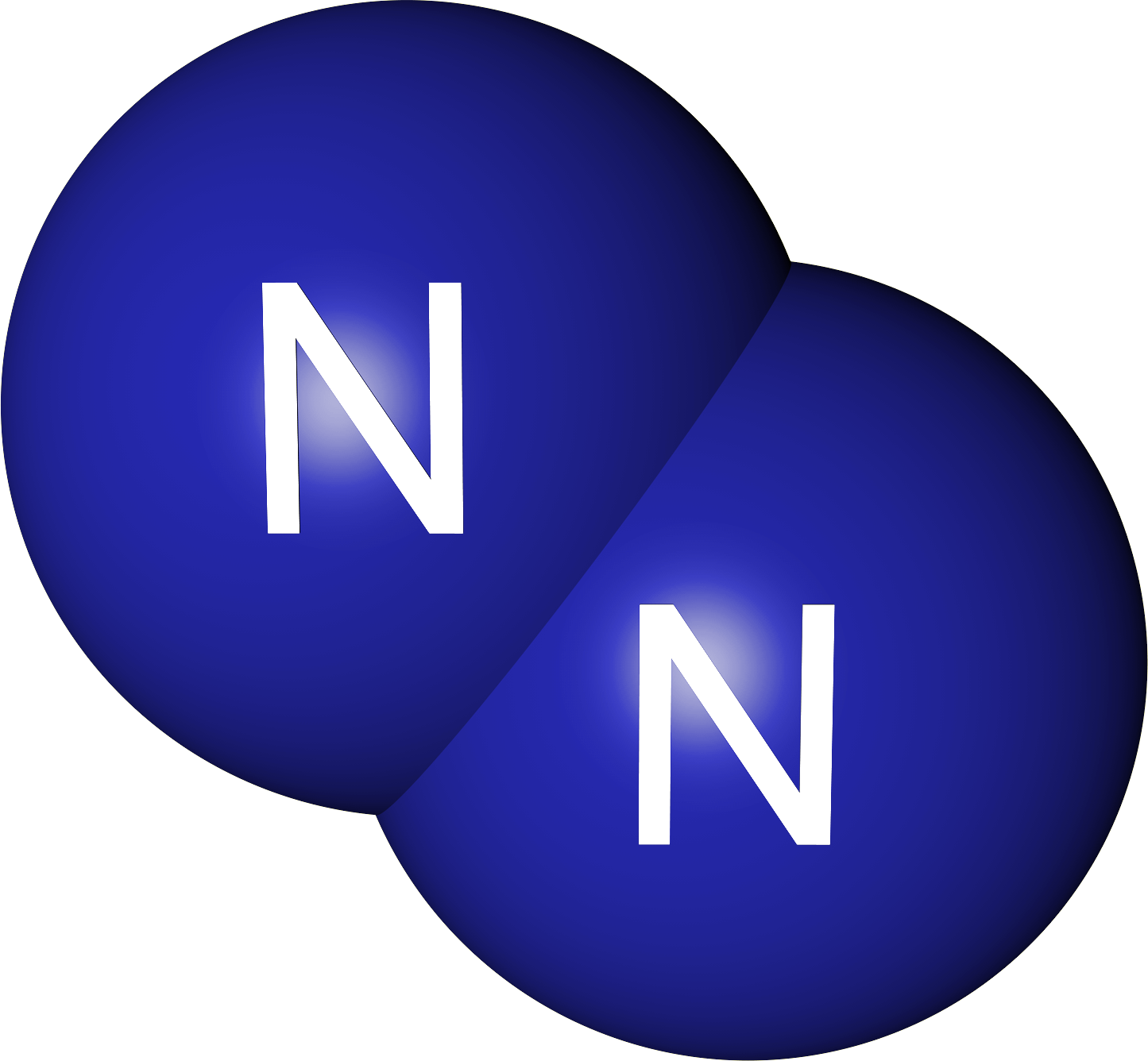
Khí Nitơ chiếm khoảng 78% và là một phần quan trọng của mọi cơ thể sống. Nitơ có hai dạng với tính ứng dụng cao, đó là khí Nitơ và Nitơ lỏng. Trong số đó, Nitơ lỏng thường được sử dụng phổ biến hơn do những đặc tính hữu ích của nó.
Cấu trúc phân tử của Nitơ N2:
- Thuộc nhóm VA với cấu trúc electron ngoài cùng là ns2np3, do đó Nitơ có tính khử và tính oxi hóa đồng thời.
- Cấu trúc electron của N2 là 1s22s22p3. Các chỉ số oxi hóa lần lượt là -3, 0, +1, +2, +3, +4, +5.
2. Tính chất lý hóa của Nitơ
2.1. Đặc tính vật lý của Nitơ là gì?
Nitơ là một chất khí không màu, không mùi, không vị, nhẹ hơn không khí với mật độ (d = 28/29). Nó trở thành dạng lỏng ở nhiệt độ -196 độ C.
Nitơ có hòa tan trong nước không? Câu trả lời là có, nhưng chỉ hòa tan ít trong nước và tạo thành dạng rắn ở nhiệt độ rất thấp. Một số người thắc mắc liệu khí Nitơ có cháy không? Câu trả lời là không, Nitơ không duy trì sự cháy và không hỗ trợ sự hô hấp.
2.2. Tính chất hóa học của Nitơ
Nitơ có EN (năng lượng ion hóa) là 946 kj/mol, vì vậy nó khá bền trong điều kiện nhiệt độ thông thường. Nitơ hoạt động chủ yếu ở nhiệt độ cao.
Nitơ có các chỉ số oxi hóa lần lượt là -3, 0, +1, +2, +3, +4, +5. Vì có các chỉ số oxi hóa bằng không, Nitơ có cả tính khử và tính oxi hóa đặc trưng hơn.

– Tính oxi hóa của Nitơ
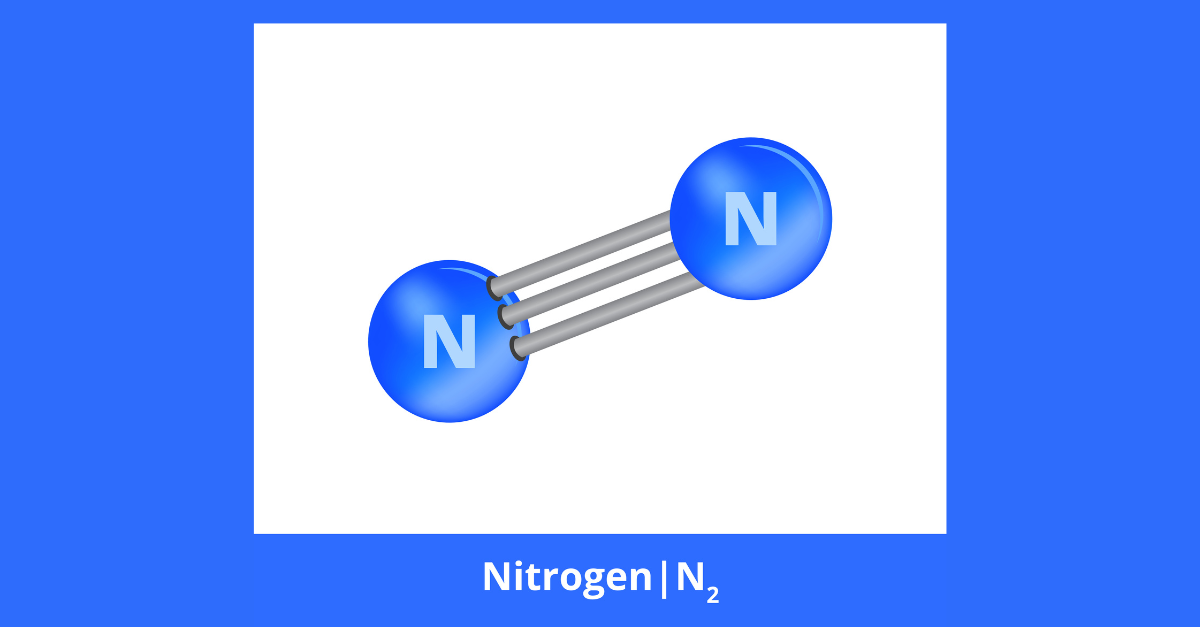
Cấu trúc phân tử của Nitơ khá ổn định với 3 liên kết và có tính oxi hóa đối với các nguyên tố hóa học như sau:
- Phản ứng với hydrogen H2
Nitơ phản ứng với hydro ở nhiệt độ và áp suất cao, với sự có mặt của chất xúc tác, kết quả tạo thành amoniac.
- Phản ứng với kim loại
Xem thêm : Khám Phá Phương Trình Nhiệt Phân Kclo3 Muối Kali Clorat
Ở nhiệt độ thông thường, Nitơ phản ứng với lithium để tạo thành nitrit. Phương trình phản ứng như sau:
6Li + N2 -> 2Li3N
Ở nhiệt độ cao, khí Nitơ phản ứng với Magiê để tạo thành nitrit magiê, phương trình như sau:
3Mg + N2 -> Mg3N2
Tuy nhiên, cần lưu ý rằng nitơ rất dễ bị thủy phân tạo ra amoniac. Nitơ chỉ có tính oxi hóa đối với các nguyên tố có độ âm điện nhỏ hơn.
– Tính khử của Nitơ
- Khí Nitơ có tính khử khi kết hợp với các nguyên tố có độ âm điện lớn hơn.
- Ở nhiệt độ khoảng 3000 độ C, Nitơ phản ứng với oxi để tạo thành monoxit Nitơ.
- Ở điều kiện thông thường, monoxit Nitơ phản ứng với oxi trong không khí để tạo thành dinitơ monoxit đặc trưng với màu nâu đỏ.
- Nitơ cũng có một số oxit khác như N2O, N2O3, N2O5, nhưng chúng không được điều chế trực tiếp từ oxi và Nitơ.
3. Trạng thái tự nhiên của Nitơ

– Trong tự nhiên, Nitơ tồn tại dưới dạng hợp chất và dạng tự do.
– Dưới dạng tự do, Nitơ chiếm khoảng 80% thể tích của không khí.
– Dưới dạng hợp chất, Nitơ có mặt trong thành phần của protein, axit nucleic và nhiều hợp chất khác. Nitơ là thành phần chính có mặt trong khoáng vật NaNO3, hay còn được gọi là diêm tiêu natri.
4. Điều chế Nitơ bằng phương pháp nào?
Nitơ được điều chế bằng cách chưng cất phân đoạn không khí lỏng, dựa trên các nhiệt độ sôi khác nhau của các chất lỏng trong không khí. Qua đó, chúng ta thu được khí bằng phương pháp đẩy nước ra.
Trong phòng thí nghiệm, ta có thể nhiệt phân muối nitrit để sản xuất Nitơ. Công thức điều chế như sau:
NH4NO2 (ở nhiệt độ cao) -> N2 + 2H2O
NH4Cl + NaNO2 (ở nhiệt độ cao) -> N2 + NaCl + 2H2O
5. Ứng dụng của Nitơ có thể bạn chưa biết
Xem thêm : Metan Ch4 Là Gì? Đặc Điểm & Ứng Dụng Quan Trọng Của Metan
Nitơ được sử dụng ngày càng phổ biến trong đời sống. Đặc biệt, khí Nitơ được sử dụng để sản xuất Nitơ lỏng.

5.1. Nitơ trong bảo quản thực phẩm
Với tính chất chống phản ứng, Nitơ ngăn chặn tốt tác động của quá trình oxy hóa. Vì vậy, Nitơ được sử dụng trong bảo quản thực phẩm.
Nitơ được sử dụng để đóng gói hoặc tách thực phẩm, giúp chống lại quá trình ôi thiu và sự tổn thất do oxi hóa.
5.2. Nitơ trong hàn ống và chế biến kim loại
Nitơ được áp dụng trong việc hàn ống và chế biến kim loại, giúp tăng độ bền và độ chắc chắn. Nitơ làm sạch ống đảm bảo an toàn và không làm hư hại cho các sản phẩm khác, nên rất được ưa chuộng sử dụng.
5.3. Nitơ trong luyện kim và chế tác kim loại
Trong ngành luyện kim và sản xuất các linh kiện điện tử, thép không gỉ, Nitơ thường được sử dụng để hỗ trợ quá trình sản xuất. Số lượng và mức độ sử dụng Nitơ phụ thuộc vào yêu cầu và đặc thù của công việc.
5.4. Nitơ trong việc bơm lốp ô tô và máy bay
Với tính chất không độ ẩm và kháng oxy hóa thấp, chỉ Nitơ được sử dụng phổ biến trong việc bơm lốp ô tô và máy bay.
5.5. Khí Nitơ trong vận chuyển thực phẩm và các sản phẩm sinh học
Khí Nitơ được sử dụng để làm lạnh trong quá trình vận chuyển thực phẩm, nhằm bảo quản các sản phẩm an toàn mà không gây hại cho thực phẩm. Nó cũng giúp bảo vệ các bộ phận cơ thể và đảm bảo sự sống của tinh trùng và trứng.
5.6. Nitơ trong lĩnh vực nghiên cứu và giáo dục
Nitơ được sử dụng trong phân tích mẫu và đóng vai trò quan trọng trong nhiều hợp chất khác nhau. Do đó, Nitơ cũng được sử dụng trong lĩnh vực nghiên cứu hóa học và giảng dạy để truyền đạt đặc tính của một số hợp chất khác nhau cho các học sinh.
FAQ – Câu hỏi thường gặp về Tìm Hiểu Nitơ Là Gì
1. Nitơ có tác dụng gì trong việc bảo quản thực phẩm?
Trong việc bảo quản thực phẩm, nitơ được sử dụng như một khí lạnh để làm giảm nhiệt độ và giảm sự tăng sinh của vi khuẩn. Nitơ có khả năng làm mát nhanh chóng và duy trì nhiệt độ thấp, giúp thực phẩm được bảo quản lâu hơn và duy trì chất lượng tốt hơn.
2. Nitơ có tác dụng gì trong công nghệ chế tạo kim loại?
Trong công nghệ chế tạo kim loại, nitơ được sử dụng làm chất phủ bề mặt để cung cấp độ bền và kháng mài mòn cho các sản phẩm kim loại. Nitơ cũng có khả năng làm tăng độ cứng của bề mặt kim loại và giảm ma sát, làm cho các sản phẩm kim loại trở nên bền hơn và có độ bóng sáng hơn.
3. Nitơ có nguy hiểm không?
Nitơ thông thường không độc hại và không gây cháy nổ khi ở dạng thông khí. Tuy nhiên, khi nitơ bị nén lại ở dạng lỏng hoặc lạnh, nó có thể gây nguy hiểm do áp suất cao và khả năng mất cân bằng nhiệt. Do đó, cần phải sử dụng nitơ một cách cẩn thận và tuân thủ các quy tắc và quy định an toàn để đảm bảo việc sử dụng nitơ an toàn.
Hãy để lại bình luận và chia sẻ bài viết Tìm Hiểu Nitơ Là Gì này nếu bạn thấy nó hữu ích! Bạn có bất kỳ câu hỏi hoặc ý kiến nào về vấn đề này, hãy để lại bình luận và chúng tôi sẽ cố gắng trả lời bạn trong thời gian sớm nhất. hoccungthukhoa.vn rất mong muốn nghe ý kiến và thông tin từ bạn để cung cấp những thông tin thú vị và hữu ích hơn trong tương lai. Cảm ơn bạn đã đọc bài viết và ủng hộ chúng tôi!
Nguồn: https://hoccungthukhoa.vn
Danh mục: Giáo Dục








Leave a Reply